Neuron特邀长篇综述:北京脑所罗敏敏团队提出抑郁“病理吸引子” 神经环路新框架
抑郁症为什么常常迁延不愈、反复发作?为什么同样的抗抑郁治疗,对不同患者效果差异巨大?这些长期困扰精神医学和神经科学的问题,正在随着神经环路研究的发展获得新的解释。
罗敏敏团队近年来围绕抑郁症神经环路机制与干预策略开展了系列研究,取得多项重要进展。基于这些研究积累,神经科学国际权威期刊 Neuron 邀请团队撰写长篇综述,对抑郁症神经环路机制研究的关键进展、核心问题和未来方向进行系统梳理。该文经过两轮同行评议后,于2026年5月5日以 "A Circuit-Based Framework for Depression: Reshaping the Pathological Attractor" 为题在线发表,提出抑郁症“病理吸引子”框架,为理解抑郁的发生、维持与干预提供了新的理论视角。

长期以来,抑郁症研究主要受单胺类递质系统异常理论主导,认为5-羟色胺、多巴胺和去甲肾上腺素等递质失衡,是抑郁发生和治疗反应的重要生物学基础。这一理论深刻影响了抗抑郁药物研发,但难以充分解释抑郁症治疗起效慢、疗效差异大、复发率高等临床现象。近年来,随着脑成像、电生理、光遗传、化学遗传、计算建模和闭环神经调控等工具快速发展,以及氯胺酮、功能连接指导下的经颅磁刺激和深部脑刺激等新型治疗手段不断出现,人们逐渐认识到,抑郁并不只是某一种递质“缺了”或某一个脑区“坏了”,而更像是整个大脑网络进入了一种异常稳定状态。
为了理解这一点,可以把大脑活动想象成一片起伏的功能地形。健康状态下,大脑能够在不同功能状态之间灵活转换;而在长期压力和异常可塑性的作用下,与负性情绪、低奖赏和低动机相关的网络状态可能形成不断加深的“吸引盆地”,使大脑活动更容易滑入其中,并难以自行脱离。在复杂系统和神经网络理论中,这种系统倾向于收敛并停留的稳定状态,被称为“吸引子”。在抑郁症中,这个吸引子不再是适应性的,而是病理性的。
基于这一思想,罗敏敏团队提出,抑郁症可被理解为一种“病理吸引子”:大脑网络在遗传易感性、慢性压力和异常神经可塑性共同作用下,逐步形成稳定、自我强化、抵抗外界扰动的病理状态。这个框架试图回答的核心问题,不只是“抑郁时哪些脑区发生异常”,而是“为什么这些异常会组织成一个持久、稳定、难以摆脱的整体状态”。
其中,一个关键推测是:抑郁状态的维持,可能来自多个尺度上正反馈回路的病理性放大。在大尺度网络层面,前扣带回(ACC)—杏仁核(BLA)、皮层—纹状体—丘脑—皮层、间脑—单胺系统等重入环路,可能不断强化负性价值、威胁偏向和奖赏迟钝;在局部环路和细胞层面,突触可塑性、神经元兴奋性以及胶质细胞调控等机制,则可能进一步改变网络增益和稳定性。正是这些相互嵌套的正反馈过程,逐渐加深病理吸引盆地,使负性情绪、低奖赏和低动机状态被持续放大并维持。
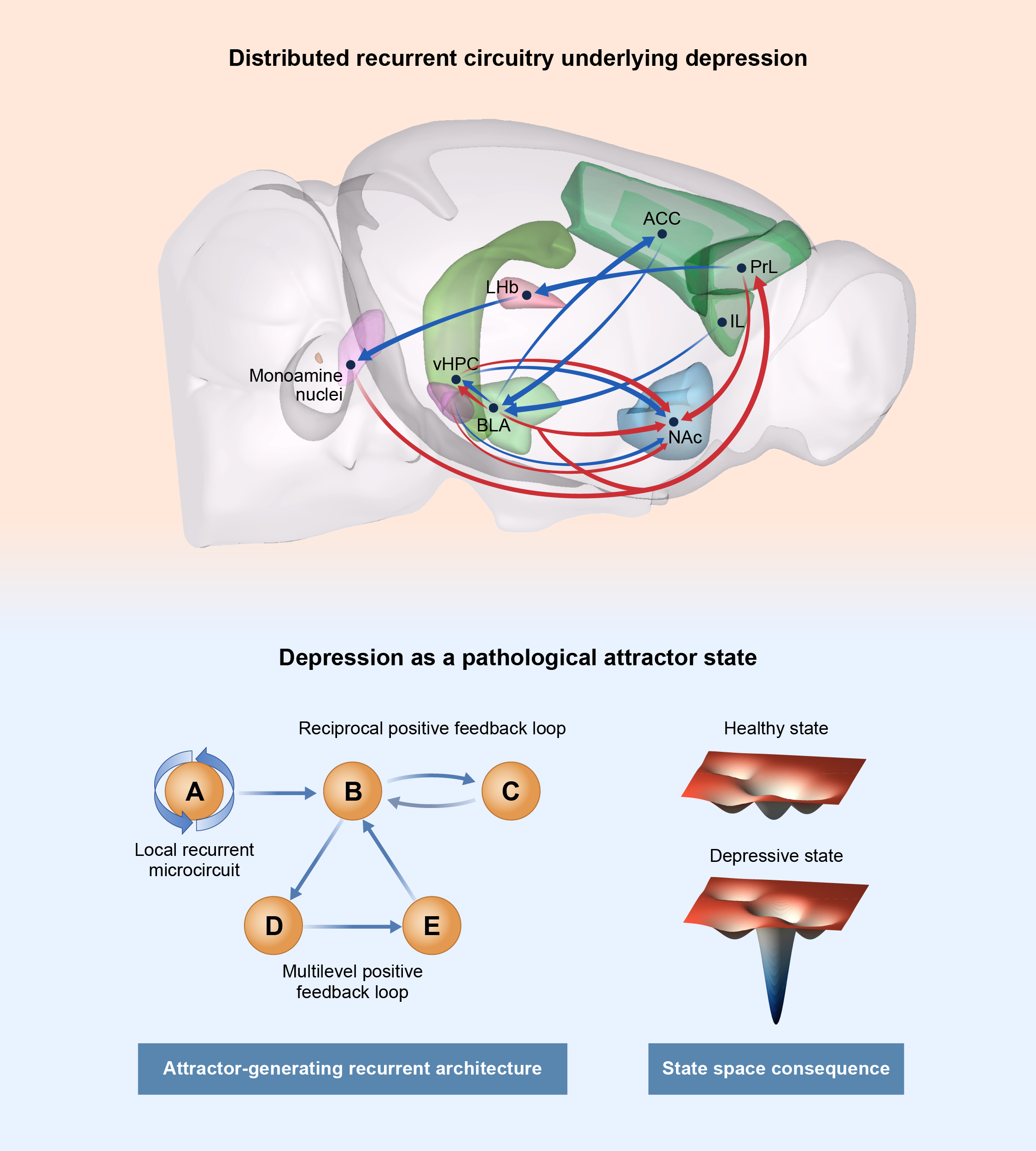
图1 大脑多尺度正反馈环路可能驱动抑郁症病理吸引子的形成与维持
在这一框架中,前额叶皮层、海马、杏仁核、伏隔核、外侧缰核以及中脑单胺系统等关键节点,共同构成抑郁相关的核心神经网络。前额叶皮层并非以简单“增强”或“减弱”的方式参与抑郁,而是呈现复杂的亚区和通路特异性失衡:部分认知控制环路功能不足,而ACC等负性价值相关通路可能过度活跃。由此,抑郁症患者之间的差异也不再只是临床“噪声”,而可能反映了不同个体脑网络状态地形的差异:不同患者或许并非陷入同一个病理吸引盆地,而是被不同深度、不同形状的病理状态所困住。
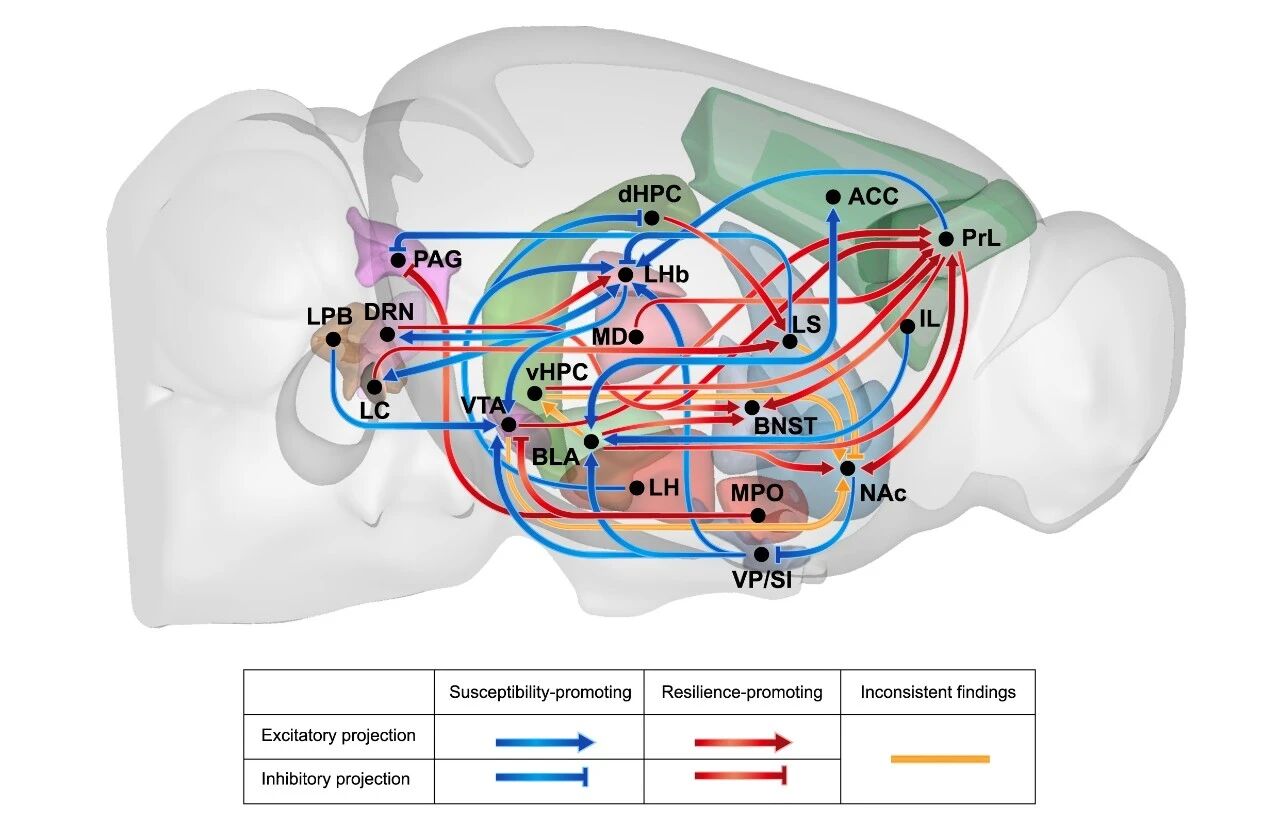
图2 抑郁症相关的神经环路互作图谱
这一视角也重新定义了抗抑郁治疗。治疗不再只是“纠正某个脑区”或“补充某种递质”,而更像是对大脑状态空间进行“拓扑工程”:改变大脑网络所处的功能地形,帮助它离开病理状态,重新进入更加适应性的状态。例如,氯胺酮等快速起效药物可能通过打开可塑性窗口,削浅病理吸引盆地,降低脑状态转换的门槛;功能连接指导下的经颅磁刺激、参数优化的深部脑刺激以及未来的闭环神经调控,则可能通过打断或重新定向病理性正反馈回路,为神经网络提供定向推动力,引导其跨越状态转换障碍。由此看来,治疗是否有效,不仅取决于“作用于哪里”,也取决于干预发生时大脑正处于什么状态。
要真正检验并发展这一框架,抑郁研究需要从静态脑图谱走向动态脑状态追踪。未来应结合纵向全脑影像、高时间分辨率电生理、多脑区长期记录与计算建模,直接刻画病理状态的停留时间、转换概率、恢复动力学和临界转折信号。在跨物种转化研究中,概率奖赏学习、奖赏贬值和基于努力的决策等任务,也将有助于在动物和人类之间建立更具可比性的行为读出,从而更好地连接神经环路机制与临床症状。
在更精细的机制层面,神经元—胶质细胞相互作用、细胞类型特异性通路和个体化环路指纹,将成为推动精准精神病学向前发展的重要支点。胶质细胞可能像缓慢变化的调节旋钮一样,改变神经网络的兴奋性、连接结构和状态稳定性;而同一脑区内不同细胞类型、不同投射通路甚至可能对行为产生相反影响。因此,在识别具有广泛适用性的关键靶点之外,未来也需要发展能够面向特定细胞类型、特定投射通路和特定脑状态的精准基因治疗与精准神经调控技术,进而更有效地重塑病理吸引盆地,推动抑郁症治疗走向更精准、更持久的个体化干预。
总体而言,“病理吸引子”框架把抑郁症治疗的目标从“被动纠正症状”推进到“主动引导脑状态转换”。这一框架的提出,不仅为整合抑郁症复杂而分散的神经环路证据提供了统一语言,也推动领域从“单一分子异常”和“局部脑区损伤”的传统解释模式,迈向以网络动力学为核心的系统性理解,并为未来发展更快速、更精准、更持久的抗抑郁干预策略奠定了新的概念基础。
论文信息
北京脑科学与类脑研究所罗敏敏博士为该研究的通讯作者,罗敏敏团队的袁正巍博士(即将入职上海交通大学心理学院)与全竞博士为共同第一作者,崔玉婷博士为本研究做出了重要贡献。该研究受中国医学科学院创新工程及医学创新基金、中国脑计划、国家自然科学基金、新基石研究员项目以及教育部基础学科和交叉学科突破计划等项目的大力支持。
原文链接:https://www.cell.com/neuron/fulltext/S0896-6273(26)00278-3



